Физико-химическое обоснование основных процессов производства метанола
окислов углерода в метанол при этом снижается с 42,2% при 6 обьемн.% СО2 до 32,7% при 12 объемн.% СО2.
Инертные компоненты. В промышленных условиях синтез метанола протекает в присутствии инертных к данному процессу газов (метан, азот). Они в реакции не участвуют и не оказывают прямого влияния на равновесие реакции образования метанола. Однако наличие их в газе снижает парциальное (эффективное) давление реагирующих веществ, что ведет к уменьшению равновесного выхода метанола. Поэтому концентрацию инертных компонентов необходимо поддерживать на минимальном уровне.
На основании изложенного следует отметить, что синтез метанола на цинк-хромовом катализаторе, который работает при 360—380 °С, целесообразно проводить только при давлениях выше 200 кгс/см2. На низкотемпературных катализаторах, эксплуатируемых в температурном интервале 220—280°С, возможна работа при давлениях ниже 100 кгс/см2, причем, чем ниже температура, тем ниже может быть и давления синтеза.
Кинетика синтеза метанола.
В гомогенных условиях (без катализатора) скорость взаимодействия окиси углерода и водорода ничтожно мала, и получить метанол в больших количествах невозможно. Для увеличения скорости реакции взаимодействия исходных компонентов используют вещества, которые, способствуя ускорению процесса, сами к концу реакций остаются химически неизменными. Для оценки этого ускорения, или иначе активности катализатора, необходимо знать скорость химического взаимодействия реагирующих компонентов. Если реакция протекает в гомогенных условиях, то скорость ее зависит от температуры, давления и концентрации реагирующих веществ. В гетерогенном, каталитическом процессе скорость реакции будет определяться также типом катализатора и состоянием его поверхности. Синтез метанола является гетерогенным каталитическим процессом, протекающим на границе раздела твердой (поверхность катализатора) и газообразной (смесь окиси углерода и водорода) фаз. До начала реакции окись углерода и водород концентрируются на поверхности катализатора (происходит адсорбция СО и Hz). Суммарный процесс синтеза метанола состоит из следующих стадий: диффузия исходных веществ к поверхности катализатора;
адсорбция этих веществ да поверхности катализатора; химическое взаимодействие адсорбированных молекул СО и Н2 до метанола;
удаление (десорбция) образовавшегося метанола с поверхности катализатора. Скорость процесса образования метанола будет равна скорости реакции в зависимости от начальных условии (температуры, давления, концентрации веществ, времени контакта газа с катализатором) позволило вывести кинетическое уравнение. Последнее используют при моделировании процесса и разработке промышленных реакторов.
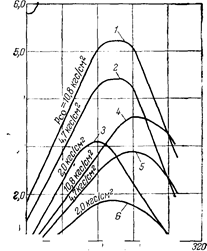
Проведенные на электронно-вычислительной машине расчеты по кинетическому уравнению показали, что оно хорошо описывает процесс образования метанола.
На катализаторе СНМ-1 и может быть использовано для расчета промышленных реакторов, работающих при 50 Krc/C можно определить оптимальные параметры процесса и равновесные условия. Наибольший выход метанола наблюдается при 255— 270° С, что согласуется с экспериментальными данными. С уменьшением парциального давления окиси углерода (повышение отношения Н2:СО) максимум активности катализатора смещается в сторону более низких температур.
Дополнительно
Технология выращивания сахарной свеклы в Сумской области
Сахарная свекла - важная техническая культура, корнеплод которой
достигает 500г и больше, содержит 19-22% сахара и более, является основным
сырьем для сахарной промышленности. Кроме сахара, в процессе переработки
корнеплодов получают ценные дополнительные продукты - мелясу и жом. Ботва
сахарной св ...
Современный прокатный стан
Современный
прокатный стан представляет собой технологический комплекс последовательно
установленных машин, используемых для получения прокатных изделий заданных
размеров с необходимыми качественными показателями. Производительность
прокатного стана определяется пропускной способностью отдельных а ...