Билеты по химии 10 класс
![]()
Органические кислоты и основания обычно являются слабыми электролитами.
Неэлектролит вообще не диссоциирует на ионы и поэтому не обладает способностью проводить электрический ток. Большинство органических соединений принадлежат к неэлектролитам. Крав мага Одесса читать дальше.
Механизм электролитической диссоциации — распада молекул или кристаллов растворяемого вещества на ионы под влиянием молекул растворителя — был понят несколько позднее. Согласно современным воззрениям, такой распад является результатом взаимодействия полярных молекул растворителя, например воды, с молекулами или кристаллической решеткой растворяемого вещества. Молекулы растворителя атакуют кристаллическую решетку, разрушая ее и переводя составные части решетки (ионы) в раствор в форме сольватированных (гидратированных) заряженных частиц Окружающие эти ионы полярные молекулы растворителя ориентированы в соответствии с зарядом ионов. Растворение электролита в известной мере упорядочивает молекулы растворителя. Естественно предположить, что эта способность к упорядочению молекул растворителя у многозарядных ионов выражена сильнее, чем у однозарядных. В этом и нужно искать причину того, что соли, содержащие многозарядные ионы, плохо растворимы (в ряде случаев практически нерастворимы) в воде. Например, хлорид бария растворим хорошо, а сульфат бария — очень плохо. Следовательно, влияние растворенного вещества и растворителя является обоюдным: полярные молекулы растворителя разрушают кристаллическую решетку растворяемого вещества на отдельные ионы, а эти ионы, переходя в раствор, вызывают изменение растворителя, заставляя его молекулы упорядочиваться. Кроме того, сольватированные ионы растворенного вещества не индифферентны по отношению друг к другу. Противоположно заряженные ионы имеют тенденцию притягиваться силами электростатического взаимодействия, образуя нейтральные молекулы или нейтральные группы молекул. Разумеется, в реальном растворе всегда присутствуют как отдельные сольватированные ионы, так и нейтральные молекулы.
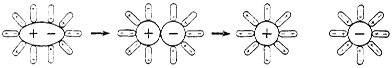
Действие растворителя на растворенное вещество настолько велико, что может вызывать электролитическую диссоциацию веществ, не обладающих ионным типом связи. Например, полярные молекулы хлороводорода, растворяясь в воде, разрываются ее молекулами на ионы. При растворении хлороводорода в бензоле, являющемся менее полярным растворителем, чем вода, диссоциации молекул не происходит. Поэтому раствор хлороводорода (кислота) в воде проводит электрический ток, а в бензоле нет.
Степень электролитической диссоциации a – число, показывающее, какая часть молекул электролита находится в растворе в виде ионов.
Согласно этому определению
![]()
Очевидно, во всех растворах неэлектролитов, где диссоциация на ионы полностью отсутствует, a=0, а в растворах, в которых все растворенное вещество присутствует в форме ионов (полная диссоциация), a=1. Очень часто для растворов средней и высокой концентраций (с»5,0% .с»10,0%) считают, что слабые электролиты характеризуются a£0,03, а сильные – a³0,30. Электролиты средней силы характеризуются промежуточными значениями степени диссоциации: 0,03£a£0,30. Однако необходимо отметить, что предложенная классификация является в значительной степени условной (особенно в случае слабых электролитов и электролитов средней силы). Это объясняется следующим. Степень диссоциации в общем случае зависит от природы электролита и растворителя, от концентрации и температуры раствора. Для растворов, образованных одними и теми же компонентами (растворителем и растворенным веществом), наибольший интерес представляет зависимость степени диссоциации от концентрации раствора. Для слабых электролитов типа H+B– (кислота) или А+ОН– (основание) степень диссоциации ос и концентрация раствора с связаны зависимостью:
![]()
где Кi — константа, характеризующая способность того или иного слабого электролита к диссоциации.
При малых значениях a (a£0,05) разность 1–a приблизительно равна 1. Тогда из этого уравнения можно получить:
![]()
что является математическим выражением закона разведения Оствальда: степень диссоциации слабого электролита в растворе тем выше, чем более разбавлен раствор.
Допустим, что при растворении электролита ВА в воде образуется раствор, имеющий концентрацию с. В результате некоторая часть а электролита ВА диссоциирует, образуя ионы B+ и А–. Величина a называется степенью диссоциации. Равновесная концентрация неионизированного электролита ВА оказывается равной с(1– a). Таким образом, можно записать
Дополнительно
Порошковая металлургия и дальнейшая перспектива ее развития
Порошковой металлургией
называют область техники, охватывающую совокупность методов изготовления
порошков металлов и металлоподобных соединений, полуфабрикатов и изделий из них
или их смесей с неметаллическими порошками без расплавления основного
компонента.
Из имеющихся разнообразных
способов ...
Нетрадиционные методы производства энергии
Рождение энергетики
произошло несколько миллионов лет тому назад, когда люди научились использовать
огонь. Огонь давал им тепло и свет, был источником вдохновения и оптимизма,
оружием против врагов и диких зверей, лечебным средством, помощником в
земледелии, консервантом продуктов, технологическ ...