Билеты по химии 10 класс
![]()
Билет №5.
Электролиты и неэлектролиты. Электролическая диссоциация неорганических кислот, солей, щелочей. Степень диссоциации.
Электролиты и неэлектролиты
Электрический ток — направленное движение заряженных частиц под действием внешнего электромагнитного поля. Подробности мкрп 340 у нас на сайте.
Заряженные частицы:
электроны — ток в металлах;
ионы — ток в растворах.
Электролиты — вещества, растворы которых проводят электрический ток: растворимые кислоты, щелочи, соли. Связь ионная или сильнополярная.
![]()
Неэлектролиты — вещества, растворы которых не проводят электрический ток: большинство органических веществ. Связь неполярная или слабополярная.
![]()
Электролитическая диссоциация
Электролитическая диссоциация — распад электролита на ионы под действием полярных молекул растворителя.
Основы теории электролитической диссоциации – С.Аррениус, 1887г.:
1. Электролиты при растворении в воде диссоциируют.
2. Под действием электрического тока ионы движутся в растворе: положительно заряженные - к катоду, отрицательно заряженные — к аноду.
3. Диссоциация – обратимый процесс
В молекуле воды связь ковалентная полярная, молекула угловая, следовательно, молекула воды — диполь.
Причина диссоциации веществ с ионной связью: диполи воды разрушают кристаллическую решетку. 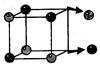
Причина диссоциации веществ с ковалентной полярной связью: молекулы воды вызывают еще большую поляризацию связи вплоть до ее разрыва.
![]()
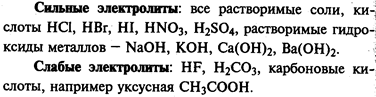
Степень диссоциации. Сильные и слабые электролиты
Степень диссоциации — отношение числа распавшихся молекул к общему числу молекул растворенного вещества:
![]()
Если а ® 1, то электролит сильный. В растворе практически нет молекул. Примеры: НСl; NaOH; KBr.
Если а ® 0, то электролит слабый. В растворе много молекул и мало ионов. Примеры: H2S; NH3; Fe(SCN)3.
Диссоциация кислот, щелочей и солей
Кислоты
— электролиты, в растворах которых нет других катионов, кроме катионов водорода.
Многоосновные кислоты диссоциируют ступенчато:
![]()
![]()
Основания
— электролиты, в растворах которых нет других анионов, кроме гидроксид-ионов.
![]()
![]()
Соли
— электролиты, в растворах которых есть катионы металлов или ион аммония и анионы кислотных остатков.
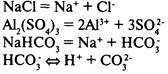
Билет №5. (углубленный)
Электролиты и неэлектролиты. Электролическая диссоциация неорганических кислот, солей, щелочей. Степень диссоциации.
Электролит проводит электрический ток в результате того, что направленное перемещение его ионов создает поток электрических зарядов. Таким образом, пропускание электрического тока через электролит сопровождается переносом вещества.
Электролитами чаще всего являются такие соединения, как кислоты, основания или соли, находящиеся в расплавленном состоянии или в водных растворах. Способность электролитов проводить электрический ток называется электролитической проводимостью. Ее следует отличать от электронной проводимости обычных проводников электрического тока, например металлов. В веществах с электронной проводимостью поток заряда обусловлен потоком электронов, а не перемещением ионов. Поэтому пропускание электрического тока через проводники с электронной проводимостью не сопровождается переносом вещества.
Электролиты в свою очередь могут быть подразделены на два типа: сильные и слабые электролиты. Сильный электролит – это соединение, которое в расплавленном состоянии или в растворе полностью ионизировано. Примером сильного электролита может служить соляная кислота. При растворении хлороводорода в воде происходит его полная ионизация:
![]()
В этом уравнении использована простая (а не двойная) стрелка, чтобы показать, что процесс идет в указанную сторону до полного завершения.
Слабый электролит – это вещество, которое диссоциирует на ионы лишь частично. Следовательно, в растворе устанавливается равновесие между недиссоциированными молекулами такого вещества и диссоциированными ионами. Примером слабого электролита является уксусная кислота:
Дополнительно
Нейросетевые методы распознавания изображений
Выполнен обзор нейросетевых методов, используемых при распознавании
изображений. Нейросетевые методы - это методы, базирующиеся на применении
различных типов нейронных сетей (НС). Основные направления применения различных
НС для распознавания образов и изображений:
применение для извлечение
...
Проектирование технологии ремонта гидроцилиндров с использованием полимерных материалов
Одно
из направлений повышения эффективности производства - его переоснащение
современной техникой, внедрение передовых технологических процессов и
достижений современной науки.
В
лесной промышленности и лесном хозяйстве таким направлением наряду с увеличением
единичной мощности выпускаемой те ...