Билеты по химии 10 класс
Химические свойства.
Атомы металлов имеют больший радиус, чем атомы неметаллов, поэтому легко теряют валентные электроны. Вследствие этого металлы проявляют восстановительные свойства.
![]()
Билет №10.
Общая характеристика неметаллов главных подгрупп IV – VII групп (IV-A – VII-A) в связи с их положением в периодической системе химических элементов Д. И. Менделеева и особенностями строения их атомов. Изменение окислительно-восстановительных свойств неметаллов на примере элементов VI-A группы.
KKK
При движении сверху вниз по группам увеличивается радиус атома и следовательно уменьшаются окислительные свойства.
Сравнительная характеристика окислительно-восстановительных свойств неметаллов на примере кислорода и серы.
Схемы электронных оболочек:
![]()
На внешнем электронном уровне атомов кислорода и серы находится по 6 электронов.
У кислорода окислительные свойства выражены сильнее, так как радиус атома меньше и валентные электроны сильнее притягиваются к ядру. Для кислорода наиболее характерна степень окисления —2, проявляющаяся при достройке внешнего энергетического уровня до 8 электронов.
Сера также может являться окислителем, проявляя степень окисления —2, но характерны также степени окисления +4 (при потере 4 р-электронов) и +6 (при потере всех шести валентных электронов).
В реакциях с металлами кислород и сера проявляют окислительные свойства, образуя оксиды и сульфиды соответственно:
![]()
В реакциях с неметаллами кислород проявляет свойства окислителя:
![]()
Сера может быть как окислителем
![]()
так и восстановителем:
![]()
Сера выступает в роли восстановителя в реакции с концентрированной азотной кислотой:
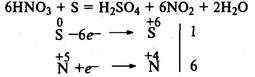
Билет №11.
Аллотропия веществ, состав, строение, свойства аллотропных модификаций.
Если какой-либо элемент может существовать в двух или нескольких твердых формах (кристаллических либо аморфных), то считается, что он проявляет аллотропию. Различные формы одного элемента называются аллотропами. Аллотропы существуют приблизительно у половины всех элементов.
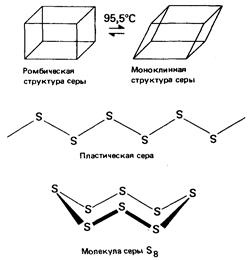
Например, углерод существует в виде алмаза либо графита. Сера существует в двух кристаллических формах - ромбической и моноклинной - в зависимости от температуры. Обе ее кристаллические формы являются примерами молекулярных кристаллов. Молекулы в них представляют собой гофрированные циклы, в каждом из которых содержится по восемь ковалентно связанных атомов серы. Твердая сера может существовать еще в третьей аллотропной форме как пластическая сера. Эта форма серы неустойчива. Она состоит из длинных цепочек атомов серы, которые при комнатной температуре разрушаются и снова образуют молекулы S8, кристаллизующиеся в ромбическую решетку.
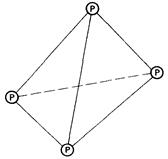
Фосфор может существовать в трех аллотропных формах. Наиболее устойчивая из них-красный фосфор. Красный фосфор имеет каркасную кристаллическую структуру, в которой каждый атом ковалентно связан с тремя другими атомами фосфора. Белый фосфор представляет собой молекулярный кристалл. Каждая его молекула содержит четыре атома фосфора, ковалентно связанных в тетраэдричес-кую структуру. Третий аллотроп - черный фосфор - образуется только при высоких давлениях. Он существует в виде макромолекулярной слоистой структуры.
Билет №12.
Электролиз растворов и расплавов солей (на примере хлорида натрия). Практическое значение электролиза.
Электролизом называются реакции в растворах или расплавах электролитов, происходящие под действием электрического тока.
В расплавах или растворах происходит диссоциация электролита. Катионы смещаются к катоду, анионы — к аноду.
Электролиз расплавов.
На катоде происходит восстановление катионов, на аноде — окисление анионов.
Электролиз расплава хлорида натрия. На катоде восстанавливаются катионы Na+ и выделяется металлический натрий, на аноде окисляются хлорид-ионы и выделяется хлор:
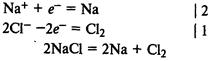
Электролиз водных растворов.
В процессах на катоде и аноде могут участвовать не только ионы электролита, но и молекулы воды.
Дополнительно
Специфика работы секретаря
Специфика работы секретаря
заключается в том, что
ему приходится не только выполнять операции с неодушевлёнными
предметами труда (документы,
технические средства), но и осуществлять многочисленные
контакты с людьми:
руководителем, сотрудниками,
посетителями, телефонными абонентами. Следует уч ...
Галактика как уровень мегамира
Актуальность,
цели и задачи ответа по настоящей контрольной работе будут обусловлены
следующими положениями. Нас интересует не только звездное население того дома,
в котором мы живем. Нас интересует и архитектура этого дома и его размеры;
интересует, как его обитатели расселены, где жилищная тесно ...