Билеты по химии 10 класс
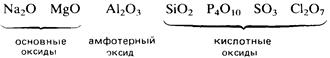
Билет №15.
Кислоты, их классификация и химические свойства на основе представлений об электролитической диссоциации. Особенности свойств концентрированной серной кислоты на примере взаимодействия с медью.
Кислота — сложное вещество, при диссоциации которого образуется только один тип катионов — ионы водорода.
![]()
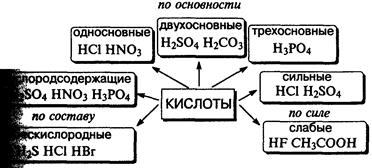
Классификация кислот.
Соляная кислота — водный раствор газа хлоро-водорода в воде.
Химические свойства.
Кислоты изменяют цвет индикаторов: лакмус окрашивается в красный цвет, метилоранж — в желтый.
При реакции с основаниями образуется соль и вода (реакция нейтрализации). В реакцию вступают как растворимые, так и нерастворимые в воде основания:
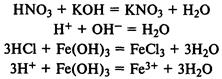
При реакции с основными оксидамиобразуются со ли:
![]()
Кислоты реагируют с металлами,находящимися в ряду напряжений до водорода, при этом выделяется газообразный водород и образуется соль:
![]()
Сильные кислоты реагирует с солями слабых кислот,
вытесняя слабые кислоты из их солей:
![]()
Получение кислот.Многие кислоты можно получить при реакции кислотных оксидов с водой:
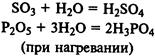

Концентрированная серная кислота
при обычной температуре не действует на многие металлы. По этой причине, например, безводная серная кислота в отличие от её растворов может сохраняться в железной таре.
Но концентрированная серная кислота действует почти на все металлы при нагревании. При этом образуются соли серной кислоты, однако водород не выделяется, а получаются другие вещества, например сернистый газ.
Так, при нагревании концентрированной серной кислоты с медью вначале серная кислота окисляет медь до окиси меди, а сама восстанавливается при этом до сернистой кислоты, которая тотчас же разлагается на сернистый газ и воду:
![]()
Образовавшаяся окись меди реагирует с избытком серной кислоты, образуя соль и воду:
![]()
Таким образом, окись меди является промежуточным веществом в этой реакции. Сложив эти уравнения, мы получим итоговое уравнение реакции, в которое входят только исходные и конечные вещества:
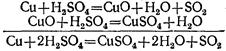
Билет №16.
Основания, их классификация и химические свойства на основе представлений об электролитической диссоциации.
Основания — электролиты, при диссоциации которых образуется только один вид анионов — гидроксид-ионы.
![]()
Классификация оснований
1. Растворимые в воде (щелочи)
— гидроксиды металлов главных подгрупп I и II групп.
![]()
2. Нерастворимые в воде
— гидроксиды остальных металлов.
![]()
Химические свойства
. Щелочи изменяют окраску индикаторов (лакмус становится синим, фенолфталеин – малиновым).
Взаимодействие с кислотами:
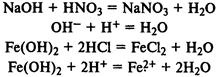
Взаимодействие с кислотными оксидами:
![]()
Растворы щелочей вступают в реакции ионного обмена с растворами солей, если образующийся при этом гидроксид нерастворим в воде:
![]()
При нагревании слабые основания разлагаются на оксиды металлов и воду:
![]()
Получение оснований.
Щелочи получают электролизом растворов солей.
Электролиз раствора хлорида натрия. Процессы на катоде и аноде:
![]()
Уравнение реакции:
![]()
Нерастворимые в воде основания получают реакцией обмена со щелочами:
![]()
Билет №17.
Дополнительно
Разработка сенсора на поверхностно-акустических волнах
В условиях
современности проблема контроля за состоянием окружающей среды выходит на все
более ведущее место. Контроль этот осуществляется как стационарными приборами, так и портативными. К стационарным приборам
можно отнести инфракрасные спектрометры, газовые хроматографы, массовые
спектрометры и ...
Технология производства мяса гусей
Животноводство - вторая
важнейшая отрасль сельского хозяйства. Она обеспечивает население
высокобелковыми и диетическими продуктами питания, а ряд отраслей промышленности
- сырьем. Особенность ее в том, что энергоемкость продукции животноводства
(затраты энергии на одну калорию продукции) в 15-2 ...