Билеты по химии 10 класс
Химическая коррозия — окисление металла без возникновения гальванической пары. Газовая коррозия — при t > 600°С:
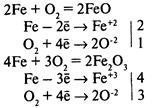
Коррозию, сопровождающуюся возникновением электрического тока за счет появления гальванической пары, называют электрохимической коррозией.
Электрохимическая коррозия – разрушение металла в электролите с возникновением гальванической пары.
![]() – ионы выходят в раствор, электроны перемещаются к менее активному металлу, например к меди.
– ионы выходят в раствор, электроны перемещаются к менее активному металлу, например к меди.
![]() – разряжаются на менее активном металле, например на меди.
– разряжаются на менее активном металле, например на меди.
Одним из наиболее широко распространенных видов электрохимической коррозии является ржавление обычной стали в водной среде и на воздухе. На поверхности металлических изделий всегда имеется пленка влаги, адсорбированной из воздуха. Она является электролитом, так как в ней растворены различные газы (СО2, SO2 и др.). Зерна карбида железа Fe3С химически менее активны, чем железо. Поэтому возникают микрогальваническис элементы: зерна Fe3С играют роль катодов, а зерна чистого железа — роль анодов. Железо разрушается — оно ржавеет. Протекающие при этом процессы весьма сложные. Укажем лишь суммарное уравнение реакции:
![]()
Ржавчина имеет неопределенный состав ![]()
Для защиты от коррозии металлов
широко используют лакокрасочные покрытия. Однако краски не вечны, изделия приходится перекрашивать. На это затрачивается ручной труд, расходуется много лакокрасочных материалов.
Из неметаллических покрытий для защиты стали и чугуна большое значение имеет эмаль. Эмаль — это силикатное стекло с добавками оксидов металлов. Ее наносят на поверхность материала в виде порошка и обжигают при 500—1000 °С.
Покрытия из эмалей обладают стойкостью по отношению к щелочам и кислотам, длительно противостоят атмосферной коррозии. Но эмаль легко разрушается при ударе. Благодаря термостойкости, декоративному виду, легкости очистки эмаль широко используется для покрытия изделий домашнего хозяйства и санитарной техники.
С целью защиты металлов от коррозии (и для декоративных целей) издавна используют металлические покрытия. Железо оцинковывают, лудят (покрывают оловом), покрывают никелем, хромируют и т. д.
Защитить металл от коррозии можно с помощью металла и другим способом. Например, если соединить железное изделие или сооружение проводником с куском более активного металла, например магния, то возникает гальванический элемент. При этом сооружение (железо) играет роль катода, а более активный металл выполняет роль анода. Анод разрушается, а катод — защищаемый металл — не изменяется. Такая защита называется протекторной.
Одним из способов борьбы с коррозией является использование ингибиторов. Это химические соединения, ничтожные концентрации которых способны почти полностью предотвращать коррозию. В некоторых случаях применение ингибиторов позволяет изготовлять аппаратуру из обычной стали вместо нержавеющей.
Одно из наиболее эффективных направлений борьбы с коррозией металлов — создание коррозионно-стойких сплавов. В больших количествах выплавляют так называемые нержавеющие стали. В их состав входят металлы (хром, никель), образующие устойчивые защитные оксидные пленки.
Билет №20.
Окислительно-восстановительные реакции (разобрать на примерах взаимодействия алюминия с оксидом железа (III), азотной кислоты с медью).
К окислительно-восстановительным реакциям могут быть отнесены химические реакции следующих типов.
Реакции замещения (вытеснения)
Примером реакций этого типа может служить реакция между оксидом железа (III) и алюминием. В этой реакции алюминий вытесняет железо из раствора, причем сам алюминий окисляется, а железо восстанавливается.
![]()
Приведем еще два примера:
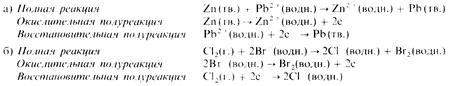
В этой реакции хлор вытесняет бром из раствора (хлор окисляется, бром восстанавливается), содержащего ионы брома.
Реакции металла с кислотами
Эти реакции, в сущности, тоже представляют собой реакции замещения. В качестве примера приведем реакцию между медью и азотной кислотой. Медь вытесняет водород из кислоты. При этом происходит окисление меди, которая превращается в гидратированный катион, а содержащиеся в растворе кислоты гидратированные протоны азота восстанавливаются, образуя оксид азота.
Дополнительно
Взаимозаменяемость, стандартиризация и технические измерения
Выполнение
данной курсовой работы преследует собой следующие цели:
–
научить студента самостоятельно применять полученное знание по курсу ВСТИ на
практике;
–
изучение методов и процесса работы со справочной литературой и информацией
ГОСТ;
–
приобретение необхо ...
Расчет релаксационного генератора на ИОУ
Разработать и рассчитать
релаксационный генератор на ИОУ
(интегральной схеме операционного
усилителя) в соответствии с данными, представленными:
·
вид генератора - мультивибратор
·
режим работы – автоколебательный
·
период следования импульсов Т, мс – 0.09
· ...